2023年11月16日,全球shou个CRISPR-Cas9基因编辑疗法获批上市,这款源于诺奖团队的药物,将人类基因治疗的高度抬上了新高度。该疗法名为Casgevy(通用名exagamglogene autotemcel,简称为exa-cel),由美国的Vertex Pharmaceuticals, Inc和瑞士的CRISPR Therapeutics联合开发,用于治疗两种遗传性血液疾病——输血依赖型β-地中海贫血(TDT)和镰刀状细胞贫血病(SCD),这是全球首个获批治疗该适应症的基因编辑疗法,也是全球首个获批应用“基因剪刀”CRISPR的疗法,为地中海贫血和镰状细胞病治疗带来巨大的进步——科学的一小步,人类的一大步。
美国FDA已授予该疗法用于治疗SCD的优先审评资格。此外,就在上月底,FDA还召集了其细胞、组织和基因治疗的外部咨询委员会,并已经对Casgevy“开绿灯”。按照日程,Casgevy针对SCD和TDT两项适应症的处方药使用者费用法案(PDUFA)日期分别为2023年12月8日和2024年3月30日。(注:PDUFA日期是指FDA审查新药的截止日期。PDUFA日期为FDA受理药物申请后10个月或6个月(如果药物被指定为优先审评)。)下面我们一起来看这款将诺奖照进现实的基因药物。
图片来源:https://www.wired.com/story/crispr-gene-therapy-approved-sickle-cell-casgevy/
地中海贫血和镰刀型贫血症的病因是人体内,血红蛋白HbB变性,影响供氧。其中,镰刀型贫血是HbB突变后结构发生变化,形成聚集的血红蛋白,把红细胞撑成镰刀状,容易堵塞血管;而地中海贫血则是HbB蛋白表达变低或者彻底没有,HbA过多,沉积在红细胞膜上。红细胞运输氧气功能也会变差。

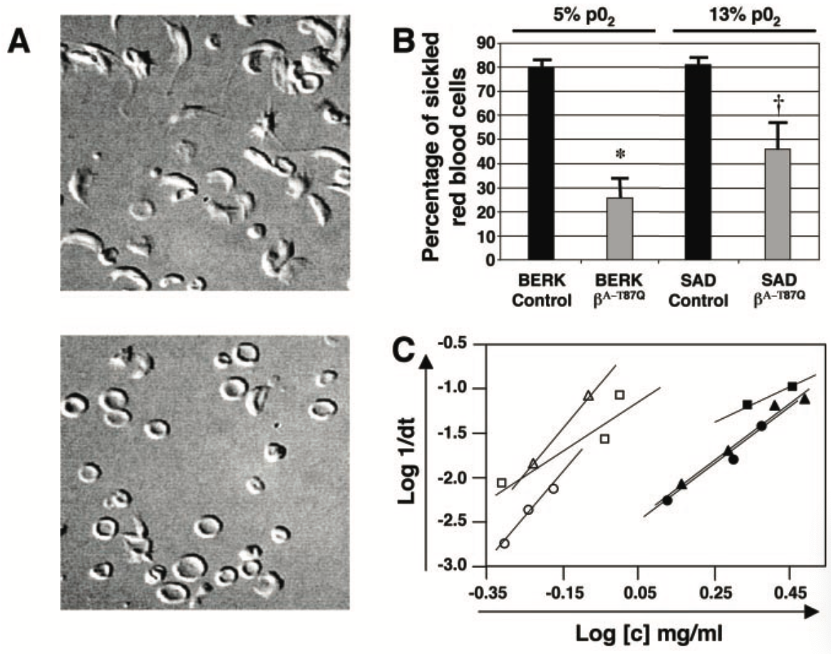
Figure:正常人的红细胞与镰刀型贫血病患者的红细胞对比图
常规的治疗手段就两种:1.输血,且频繁输血一辈子;2.造血干细胞移植,通过基因编辑,修正后的,载有正常HbB的造血干细胞。最早针对TDT和SCD的治疗,可以追溯到1982年,以小鼠为实验动物模型,探索疾病的治疗手段;1996年,开始使用慢病毒为载体,提送外源基因;2006年,基因治疗进入临床试验阶段,2008年,第一例TDT患者治愈;2015年,第一例SCD患者治愈。
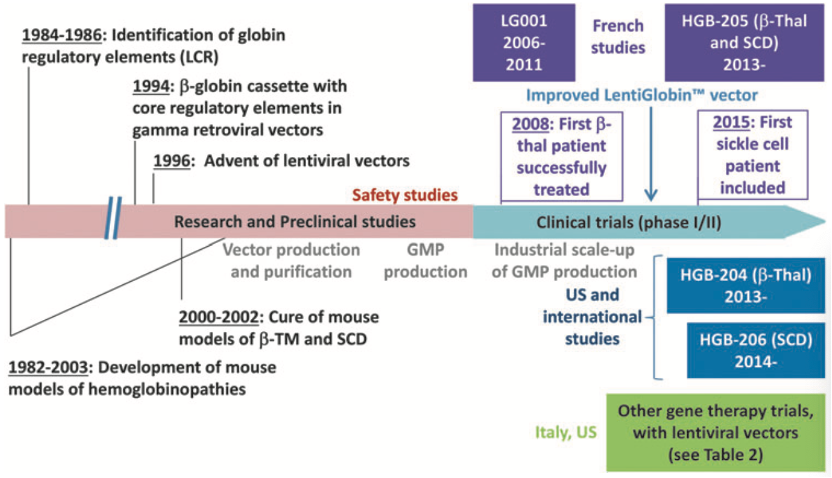
Figure:慢病毒的优化改进,与TDT和SCD的治愈相伴而行
科学家提出,既然HbA和突变HbB无法配对,那么从患者体内分离出造血干细胞,借助慢病毒将HbA(T87Q)整合入干细胞的DNA内,再把造血干细胞回输体内,分化出正常的红细胞运输氧气,于是美国Bluebird公司的Zynteglo诞生了[1]。该药物同样对镰刀型贫血症有效[2]。想了解更多基因治疗的药物,可以回看吉凯基因10月的直播。
但Zynteglo也存在致命问题——借助慢病毒递送外源基因,这段外源基因会随机整合入宿主细胞的基因组中,插入位点不可控,有致癌风险。在临床试验的过程中,两位患者出现了骨髓细胞异常增生(MDS)和急性髓系白血病(AML),尽管后续经过验证,该并发症与慢病毒基因组的随机插入没有明显相关性,但依旧存在外源片段基因整合的风险。
也有科学家尝试了基因敲入技术(KI),将正常基因定点插入,但是效率很低,随即科学家把研究思路放在了另一个亚型的血红蛋白HbF上。

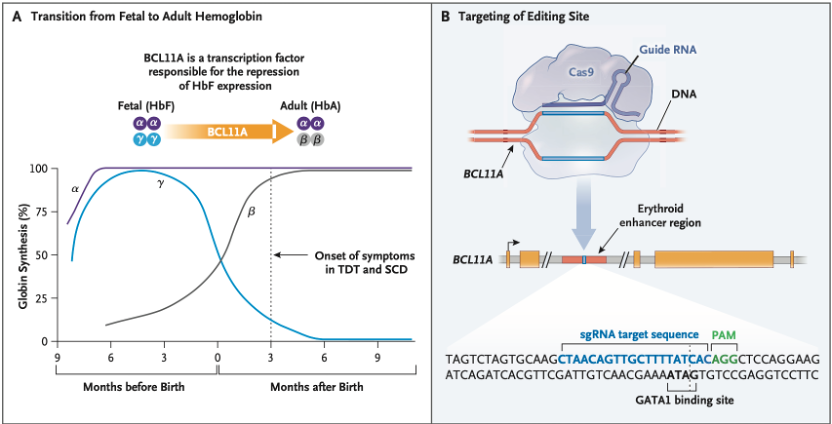
Figure:Casgevy原理——借助CRISPR-Cas9敲低Bcl11a,释放HbF
在胎儿时期,HbF是运输氧气的血红蛋白,但成年后,HbF基因被Bcl11a因子关闭,导致成年人没有HbF[3]。于是科学家提取了患者造血干细胞,体外借助CRISPR-Cas9,敲除了Bcl11a,释放了HbF,再将基因敲除后的造血干细胞回输至患者体内,从而让患者永久产生HbF,不再输血治疗。
药 物 开 发
CRISPR Therapeutics作为美股市值最高的基因编辑公司,2013年,由日后的诺奖得主Emmanuelle和其合伙人在波士顿创立。该公司的研究人员发现,CRISPR/Cas9“基因剪刀”,基于这项技术,研究人员可以极其精确地改变动物、植物和微生物的DNA。
Vertex和CRISPR Therapeutics两家公司合作开发了基因编辑。但难点颇多,需要逐个击破,例如:造血干细胞的获取及体外培养,sgRNA和Cas9的生产,提送工具,检测基因编辑是否脱靶,基因插入位点的检测等;此外,临床上也存在安全隐患,回输造血干细胞前,需要做化疗清髓,一方面影响生殖干细胞,导致不孕不育;另一方面,清髓后免疫缺乏,患者容易感染。
那又怎么样呢?困难只是懦夫的绊脚石,确是勇士成功路上的垫脚石。
Figure:法国的科学家埃马纽埃尔·卡彭蒂耶(Emmanuelle Charpentier)和来自美国的科学家珍妮弗·安妮·道德纳(Jennifer A. Doudna)将诺奖照进现实
临 床 试 验
实验是检验真理的金标准。临床实验中,患者回输了自身被基因编辑过的造血干细胞,被重新激活的HbF替代了突变的HbB,完成运输氧气的工作,且患者在回输造血干细胞的12个月内,不太需要输血,达到临床终点。回顾性分析CTX-001的一期临床数据,不同患者产生的HbF量不均一,说明基因敲除策略,目前无法做到HbF基因表达的精准调控[4]。
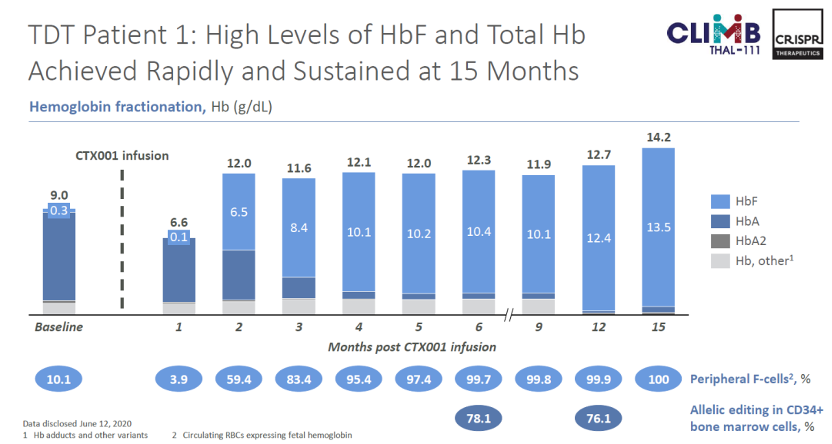
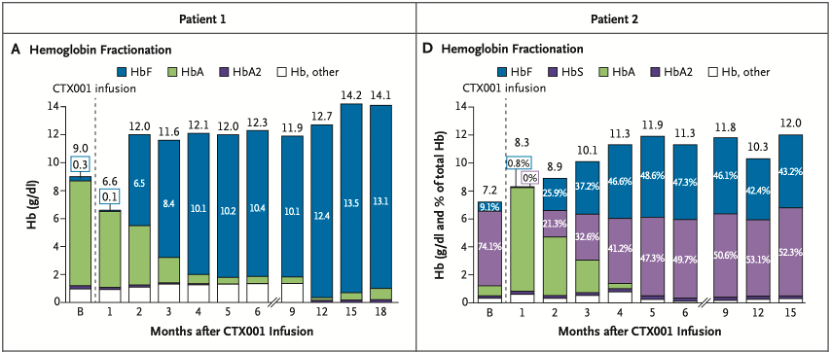
Figure:TDT患者的临床数据,在接受一次性CTX001治疗2个月后,摆脱了对于输血的依赖,且表现出了强劲、持久的HbF表达
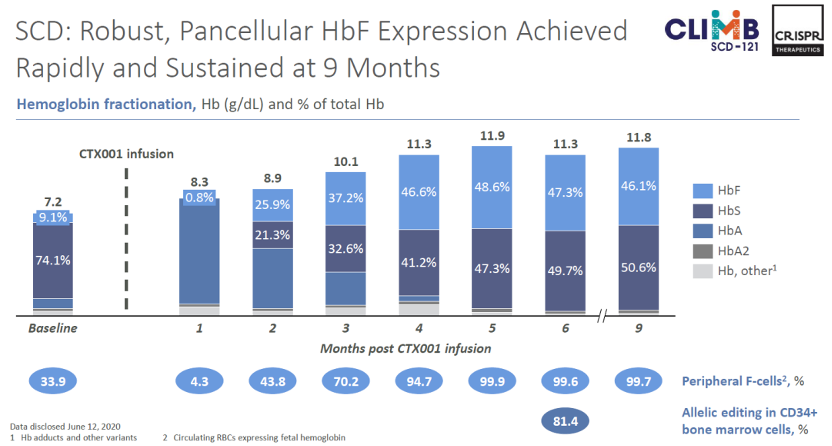
Figure:SCD的临床治疗数据,来源CRISPR Therapeutics的报告
在SCD的临床试验中,患者此前每年平均发生7次血管堵塞(血管闭塞危机),但在治疗的9个月期间,患者没有发生过1次堵塞。并且同样在单剂量输注CTX001后,患者体内快速实现了强劲、持久、泛细胞HbF高水平表达。
小 结
罗马并非一天建成,TDT和SCD的治疗也并非一蹴而就。从1982年探索出TDT和SCD的病因;到1996年尝试用慢病毒递送外源基因,来修复造血干细胞;到2006年,针对TDT和SCD进入临床试验阶段;到2013年,日后的诺奖得主Emmanuelle,在美国波士顿创立CRISPR Therapeutics公司;到2019年,美国Bluebird公司的Zynteglo上市;到2020年,诺贝尔化学奖颁给了法国的科学家埃马纽埃尔·卡彭蒂耶(Emmanuelle Charpentier)和来自美国的科学家珍妮弗·安妮·道德纳(Jennifer A. Doudna);到2023-11-16,诺奖照进现实,体外基因编辑的Casgevy成功获批在欧洲上市。笔者相信明年,用于治疗甲状腺素转运蛋白淀粉样变性的体内CRISPR基因编辑疗法——NTLA-2001也会上市。
参考文献:
1. Negre O, Eggimann AV, Beuzard Y, Ribeil JA, Bourget P, Borwornpinyo S, Hongeng S, Hacein-Bey S, Cavazzana M, Leboulch P, Payen E. Gene Therapy of the β-Hemoglobinopathies by Lentiviral Transfer of the β(A(T87Q))-Globin Gene. Hum Gene Ther. 2016 Feb;27(2):148-65. doi: 10.1089/hum.2016.007. PMID: 26886832; PMCID: PMC4779296.
2. Pawliuk R, Westerman KA, Fabry ME, Payen E, Tighe R, Bouhassira EE, Acharya SA, Ellis J, London IM, Eaves CJ, Humphries RK, Beuzard Y, Nagel RL, Leboulch P. Correction of sickle cell disease in transgenic mouse models by gene therapy. Science. 2001 Dec 14;294(5550):2368-71. doi: 10.1126/science.1065806. PMID: 11743206.
3. Sankaran VG, Menne TF, Xu J, Akie TE, Lettre G, Van Handel B, Mikkola HK, Hirschhorn JN, Cantor AB, Orkin SH. Human fetal hemoglobin expression is regulated by the developmental stage-specific repressor BCL11A. Science. 2008 Dec 19;322(5909):1839-42. doi: 10.1126/science.1165409. Epub 2008 Dec 4. PMID: 19056937.
4. Frangoul H, Altshuler D, Cappellini MD, Chen YS, Domm J, Eustace BK, Foell J, de la Fuente J, Grupp S, Handgretinger R, Ho TW, Kattamis A, Kernytsky A, Lekstrom-Himes J, Li AM, Locatelli F, Mapara MY, de Montalembert M, Rondelli D, Sharma A, Sheth S, Soni S, Steinberg MH, Wall D, Yen A, Corbacioglu S. CRISPR-Cas9 Gene Editing for Sickle Cell Disease and β-Thalassemia. N Engl J Med. 2021 Jan 21;384(3):252-260. doi: 10.1056/NEJMoa2031054. Epub 2020 Dec 5. PMID: 33283989.
